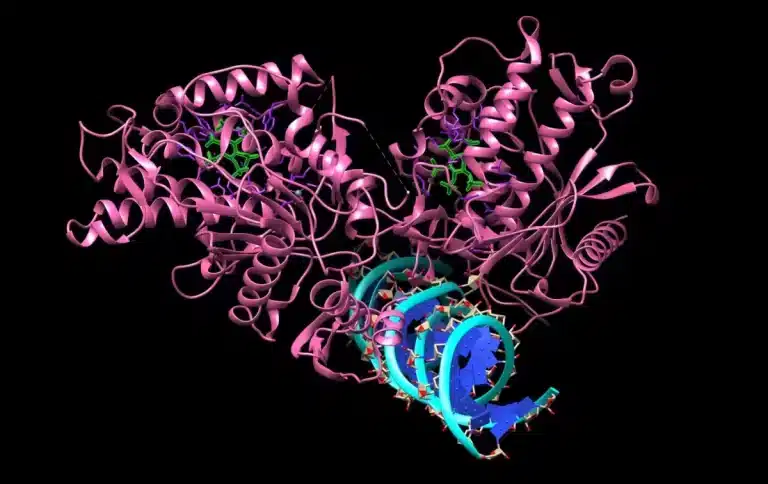
La mitad del Nobel de Química 2024 concedido a Demis Hassabis y John Jumper reconoce el inicio de una nueva era en el conocimiento de los seres vivos.
No es difícil dimensionar la gran importancia científica que tiene la predicción de la estructura de las proteínas, el descubrimiento que les valió el premio Nobel de Química 2024 a Demis Hassabis y John Jumper, quienes no son químicos sino desarrolladores de Inteligencia Artificial.
Se puede decir, por ejemplo, que la mitad del premio que les correspondió es uno de los Nóbeles que más pronto se han entregado, pues el artículo donde reportaron el hallazgo se publicó en la edición del 15 de julio de 2021 de la revista Nature, y apenas tres años después recibieron el premio; cuando el tiempo de espera promedio entre publicar un descubrimiento y recibir el premio es de 22.3 años.
Ciertamente, la otra mitad del premio, la que le correspondió a David Baker, fue un poco más tardada, pues el reporte de su investigación pionera para diseñar enzimas de novo (y no con base en las naturales) se publicó en Science en 2008. Pero sin duda fue una buena idea empaquetar ambos hallazgos, ya que el primero tiene relevancia científica y el segundo, que explicaré en una entrega posterior, abre la puerta a uno tremendo campo para biotecnología, aunque la hace un poco menos biológica.
Las proteínas, trabajadoras esenciales
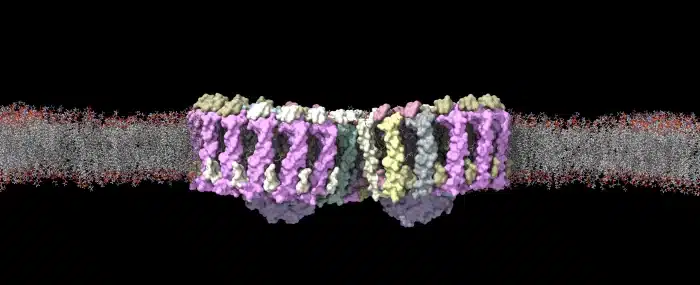
Un ser vivo puede ser definido por unas cuantas características, que curiosamente corresponden a los diferentes tipos de macromoléculas que lo componen, y en ellas las proteínas juegan un papel que si no es el más importante sin duda es el más grande. La primera característica es que el ser vivo es distinto y está separado del medio en que vive, lo cual se logra, a pequeña a escala, por la membrana celular formada por grasas (lípidos es su nombre más formal).
Otra característica destacable de los seres vivos es que se pueden reproducir y dar origen a otro u otros seres tan vivos como ellos y muy similares, casi idénticos, pero no necesariamente. En ese caso, la información que permite que los nuevos seres vivos sean similares al progenitor, y que cuando muta puede generar las diferencias, está almacenada en las grandes cadenas de ADN.
Todas las demás características de los seres vivos están a cargo de las proteínas. La respiración para obtener energía; todo lo que tiene que ver con el movimiento, desde los cilios de los paramecios hasta el impulso nervioso y la contracción muscular en animales pluricelulares; casi todo lo que se relaciona con las estructuras (salvo las lipídicas) ya sea por el lado de la construcción o por lo “bloques” con que ésta se haga…
La realización de la fotosíntesis en las plantas y la alimentación en los animales están a cargo de las proteínas; en nuestro caso, como seres humanos, las proteínas determinan desde el color del iris hasta la contracción muscular, funcionan como hormonas, sustancias señalizadoras, anticuerpos, e incluso hay proteínas diseñadas para ser comidas, como la caseína de la leche… No es exageración decir que hacen prácticamente todo.
De hecho, la información que se guarda en el ADN, y que determina cómo es un ser vivo, se traduce en cómo hacer las distintas proteínas que se encargarán de constituir al ser vivo y de sus funciones y características.
Forma y función
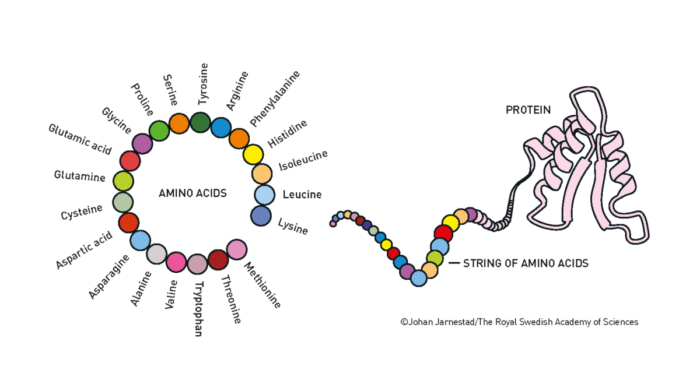
Las proteínas se componen de 20 aminoácidos diferentes enlazados uno detrás de otro en largas cadenas de diferentes combinaciones (el orden lo determina el ADN). La función que desempeñan en el ser vivo, si van a ser estructurales como la queratina de las uñas o del pelo o si van a ser insulina que señaliza que toca almacenar glucosa, depende únicamente de la forma tridimensional que adopte la cadena de aminoácidos.
Conocer la forma de una proteínas es difícil, dado su pequeño tamaño no hay manera de crear un microscopio que permita verlas; sin embargo, a finales de la década de los 50s, John Kendrew y Max Perutz (Nobel de Química en 1962) desarrollaron la cristalografía de rayos X, una técnica que permite inferir estructuras tridimensionales moleculares por medio de cálculos a partir de un “patrón de difracción”.
No hace falta decir que esto es muy complicado y laborioso, empezando porque no es fácil cristalizar las proteínas y siguiendo porque el patrón de difracción no es una forma sino un montón de claroscuros que se deben procesar e interpretar matemáticamente para obtener una idea de la forma.
En 1961, Christian Anfinsen descubrió, que la estructura tridimensional de una proteína está “completamente determinada” por su secuencia de aminoácidos. El Premio Nobel de Química se le concedió en 1972.
Dado que, desde los años 70 del siglo pasado, es posible secuenciar los genes en el ADN y saber a qué cadena de aminoácidos dan origen, surgió la idea de que debería ser posible predecir la estructura tridimensional de una proteína a partir de su secuencia de aminoácidos. Eso es lo que lograron Hassabis y Jumper con la IA DeepMind.
El papel de la IA
Desde que tenía cuatro años, Demis Hassabis comenzó a jugar ajedrez, y alcanzó el nivel de maestro a los 13 años. Pero no se dedicó a jugar, sino que en su adolescencia comenzó una carrera como programador y desarrollador de juegos. Más tarde, entró a los campos de la inteligencia artificial y la neurociencia, “donde hizo varios descubrimientos revolucionarios”, señala el sitio del Nobel.

En 2010 cofundó DeepMind, una empresa que desarrollaba modelos de IA para juegos de mesa populares que en 2014 fue vendida a Google. Dos años más tarde, DeepMind logró vencer en cuatro de cinco juegos a Lee Se-dol, gran maestro de Go, un juego de mesa que se consideraba un gran reto para la IA porque, a diferencia del ajedrez, antes que millones de cálculos requería de dos cosas que no se pueden programar y casi ni siquiera definir con precisión: intuición y creatividad.
Aunque Lee Se-dol quedó devastado por su derrota, el Go no era el objetivo de Hassabis, sino un medio para desarrollar mejores modelos de IA. Después de la victoria de DeepMind, en 2018, el equipo estaba listo “para abordar problemas de mayor importancia para la humanidad”, por lo que se inscribió en la decimotercera competición de la Evaluación Crítica de la Predicción de la Estructura de las Proteínas (CASP por su sigla en inglés).
Con su modelo de IA, AlphaFold, el equipo de Hassabis aventajó a los intentos previos, pues alcanzó casi el 60% de precisión en sus predicciones, en comparación con la estructura objetivo; mientras que en años anteriores en CASP se había logrado una precisión del 40%, en el mejor de los casos. Pero para tener éxito en la Evaluación, la predicción debía tener una precisión del 90 por ciento.

Para dar el último paso, el equipo tuvo que esperar la llegada del físico y matemático John Jumper, quien cambió su interés por el universo por las proteínas, que podían ayudar a resolver problemas médicos, después de trabajar en una empresa que utilizaba súper computadoras para simular dinámica de proteínas.
En 2017, recién terminado su doctorado, Jumper escuchó rumores de que Google DeepMind había comenzado, en gran secreto, a predecir las estructuras de las proteínas. Les envió una solicitud de empleo. Las contribuciones de Jumper fueron decisivas para el desarrollo de AlphaFold2, la IA con que el equipo de Hassabis y Jumper no sólo ganó el CASP, también los premios Fronteras del Conocimiento a principios de 2024 y ahora el Nobel.
Antes de concluir, tengo que señalar que para entrenar a AlphaFold y AlphaFold2se utilizaron las imágenes de alrededor de 200 mil proteínas diferentes obtenidas con mucho esfuerzo y con, principalmente, cristalografía de rayos X, pero también con otros métodos desarrollados en los últimos años.
Epílogo futurista
“… plegamos las 200 millones de proteínas conocidas por la ciencia y pusimos esas estructuras a disposición de cualquier persona del mundo para que las use”. Demis Hassabis en X.
Una vez que AlphaFold2 estuvo listo, Hassabis y su equipo lo usaron para averiguar la estructura tridimensional de las 200 millones de proteínas de las que se conoce la secuencia de aminoácidos y, según comenta, en su cuenta de X, las pusieron disponibles públicamente en colaboración con el European Bioinformatics Institute (EMBL-EBI).
A la fecha, “(m)ás de 2 millones de investigadores ya han utilizado AlphaFold2 y sus predicciones para avanzar en una amplia gama de trabajos importantes, desde el diseño de enzimas hasta la comprensión de enfermedades y el descubrimiento de fármacos”, añade Hassabis.
La enorme ventaja que tienen las predicciones estructurales de AlphaFold2 sobre las imágenes de cristalografía, además de que permiten saber la estructura de las proteínas, es permiten hacer simulaciones dinámicas del comportamiento de las proteínas y no se limitan a la obtención de una imagen congelada.
Así, no es difícil predecir que el trabajo de Hassabis, Jumper, AlphaFold2 y quienes les sigan significará una revolución en el conocimiento que tenemos de los seres vivos a nivel molecular. El trabajo de David Baker, que explicaré con detalle en una próxima entrega, será también una revolución en la biotecnología.